国家市场监督管理总局2020年5月20日发布公告,根据《食品安全法》规定,瑞士乳杆菌R0052等4种新食品原料、三赞胶等21种食品添加剂新品种、辛酸锌等28种食品相关产品新品种已顺利通过专家技术审评,公开征求意见后,获得公告,从此为其合法合规生产及生产应用提供依据。由OCI负责申报的一款食品添加剂新品种也名列其中。凭借丰富的申报经验、精准的法规解读以及强大的食品专业技术背景团队,OCI食品团队负责的食品添加剂新品种申报从日常KPI跟进、申报材料撰写、专家资源互动,到最后协助答辩,整个申报过程的紧密节奏大大缩短了申报周期,为企业节约了宝贵的时间成本。鉴于此次公告获批产品较多,小编将分三次为您带去产品信息分析并分享申报经验,为潜在有需求的食品企业提供宝贵的、可借鉴的技术指导。
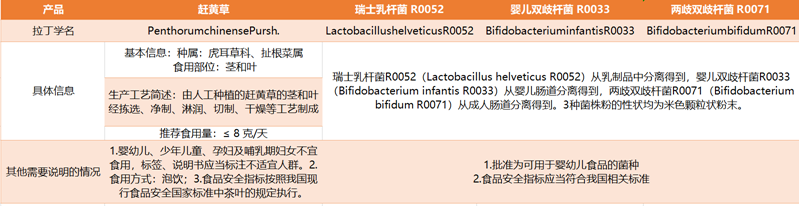
一、获批新食品原料信息汇总
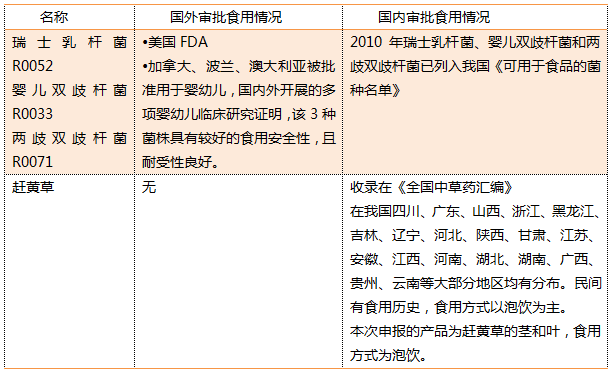
二、获批新食品原料国内外审批及食用情况
三、新食品原料申报分享
在咨询新食品原料申报的过程中,很多企业比较关心中药材类、或是微生物类的新食品原料申报的重点和难点是什么?是否比提取物类的原料申报难度大? 其实无论什么类型的新食品原料,该原料在预期食用量和预期使用条件下的安全性是申报时应最先满足的条件。
那么,如何判定物质的安全性?该原料作为食品供人类食用的安全历史是最直接有力的证明,通过科学评估的手段论证其作为食品原料的安全性是其依据。这样的评估方式和欧美发达国家评估新食品原料(如美国的GRAS和欧盟的Novel Food)的原则是一致的。根据《新食品原料申报与受理规定》,‘科学的安全评估’在新食品原料申报材料中具体表现为:
✔ 成分分析报告
✔ 卫生学检验报告
✔ 毒理学评价报告
✔ 安全性评估意见
✔ 微生物耐药性试验报告和产毒能力试验报告
✔ 其他辅助安全性评估的资料
目前,微生物类的新食品原料申报需要做耐药、产毒测试,加以验证其安全性,该类原料在国内外的审批及应用较多,人类对其的探索也将是一个长期、严谨、科学的过程。
中草药类的新食品原料是具有中国特色的一类原料,符合中国人民长久以来‘食疗’、‘药膳’的传统理念。虽然这样的原料在国外审批及应用较少,但是中草药类的物质在当地(局部)的使用和食用历史是很好的申报入手点。
最后,OCI建议,企业在申报时应通过充足的实验、数据、文献研究等材料论证该原料在预期使用条件下作为食品的安全性。另一方面,企业应积极结合当地产业或行业特色,借助当地政府的力量共同推进申报的进展。